近日,广东省人民医院/广东省肺癌研究所杨衿记教授团队联合创芯国际在 Thoracic Cancer杂志上发表了一项回顾性临床及转化医学研究Clinical outcomes of EGFR+/METamp+ vs. EGFR+/METamp- untreated patients with advanced non-small cell lung cancer 。该研究通过对EGFR敏感突变合并或不合并原发MET扩增的晚期NSCLC患者数据及利用肺癌患者恶性胸腔积液建立的肺癌类器官(Lung cancer organoid,LCO)模型进行分析,旨在评估这些患者一线接受EGFR-TKI单药治疗的临床疗效和生存预后及双靶联合治疗方案是否能进一步改善这部分患者的临床结局。
研究结果进一步证实了EGFR-TKI单药治疗作为EGFR+/MET amp+晚期NSCLC患者的一线治疗方案,临床预后不佳,而通过肺癌类器官模型和患者后线双靶向治疗临床数据,研究团队发现双靶联合治疗方案对该类患者将更有效。这些发现将通过在研的前瞻性、随机对照临床试验来验证。
MET失调与EGFR-TKI治疗的原发性和继发性耐药相关。然而,携带EGFR敏感突变和原发MET 扩增的患者临床病理学特征和临床结局仍有待探索。患者来源肿瘤类器官模型可再现肿瘤的异质性和多样性,在基因型和表型上与临床标本高度一致,并能在体外模拟抗肿瘤药物的临床疗效,为临床治疗提供有价值的参考。
本研究共纳入54例携带EGFR敏感突变合并MET过表达的非小细胞肺癌患者。其中40例患者根据荧光原位杂交技术(Fluorescence in situ hybridization,FISH)的结果被分为两组:EGFR+/METamp-组(n = 22)和EGFR+/METamp+组(n = 18),作者回顾性地分析了这些患者接受一线EGFR-TKI治疗后的生存结局。同时,利用两种不同患者来源的恶性胸腔积液建立LCOs,并进行体外药物敏感性试验,以评估患者肿瘤抑制率和药物治疗的敏感性。
研究结果
Typical case 1:
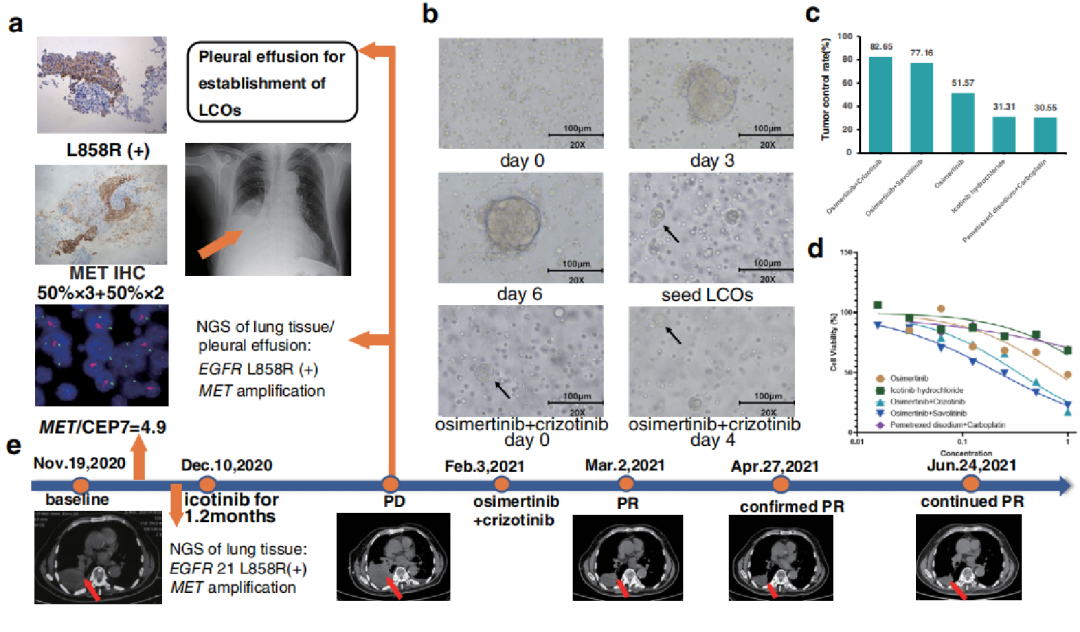
图1. EGFR+/METamp+患者双靶向临床反应和类器官模型
一名被诊断为晚期肺腺癌并同时携带EGFR exon21 L858R突变和原发MET过表达的患者,在接受1.2个月的一线埃克替尼治疗后出现原发性耐药,研究团队收集了患者此时的恶性胸腔积液。同时,对患者一线埃克替尼治疗前的活检组织样本进行回顾性MET FISH检测。FISH检测结果发现患者合并原发MET扩增(MET/CEP7=4.9),表明该患者是EGFR+/ METamp+肺腺癌患者。
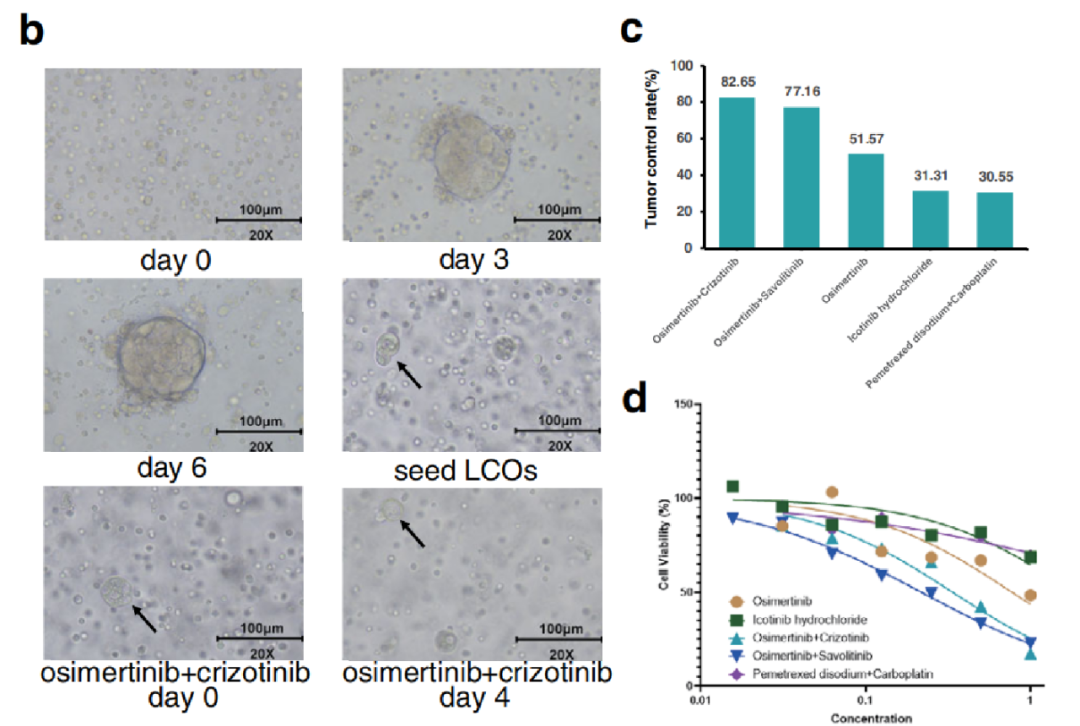
图2. (b) LCOs培养及药敏形态图。(c) 5种不同抗肿瘤药物方案(奥希替尼+克唑替尼/奥希替尼+赛沃替尼/奥希替尼单药/埃克替尼单药/培美曲塞+卡铂)对LCOs的抑制率。(d) LCOs对5种不同抗肿瘤药物方案处理的剂量-反应曲线。
在对来自患者恶性胸腔积液的LCOs进行的体外药物敏感性试验中,半抑制浓度(IC50)值表明患者可能对奥希替尼和MET-TKI的联合治疗具有潜在的更佳疗效。因此,该患者从2021年2月开始接受EGFR-TKI和MET-TKI的双靶联合治疗作为二线治疗。1个月后肿瘤病灶出现了显著应答,最佳反应是PR。在数据收集期结束时,该患者仍受益于该双靶联合治疗方案,表明由患者恶性胸腔积液建立的LCO模型的药敏试验结果与临床肿瘤应答之间的一致性,同时该模型可用于预测一线埃克替尼治疗发生耐药后,患者对奥希替尼和克唑替尼联合治疗的临床疗效。
Typical case 2:
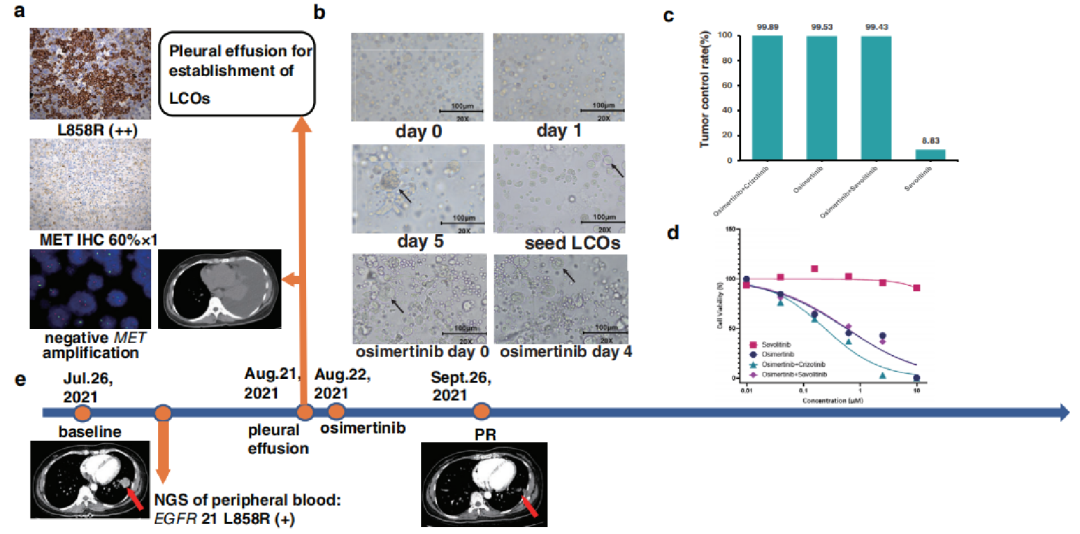
另外一名同样携带EGFR exon21 L858R突变却不合并MET扩增的EGFRm晚期肺腺癌患者,研究团队同样利用其恶性积液构建了LCO模型。体外药物敏感性试验的结果显示患者对奥希替尼治疗的潜在疗效,此外在该患者的LCOs中,MET-TKI(赛沃替尼或克唑替尼)和EGFR-TKI(奥希替尼)的双重靶向联合治疗并没有增强奥希替尼单药的抗肿瘤活性。因此,该患者接受了一线奥希替尼单药治疗,疗效达到了PR。表明LCO模型可用于预测患者对奥希替尼一线治疗的临床疗效。
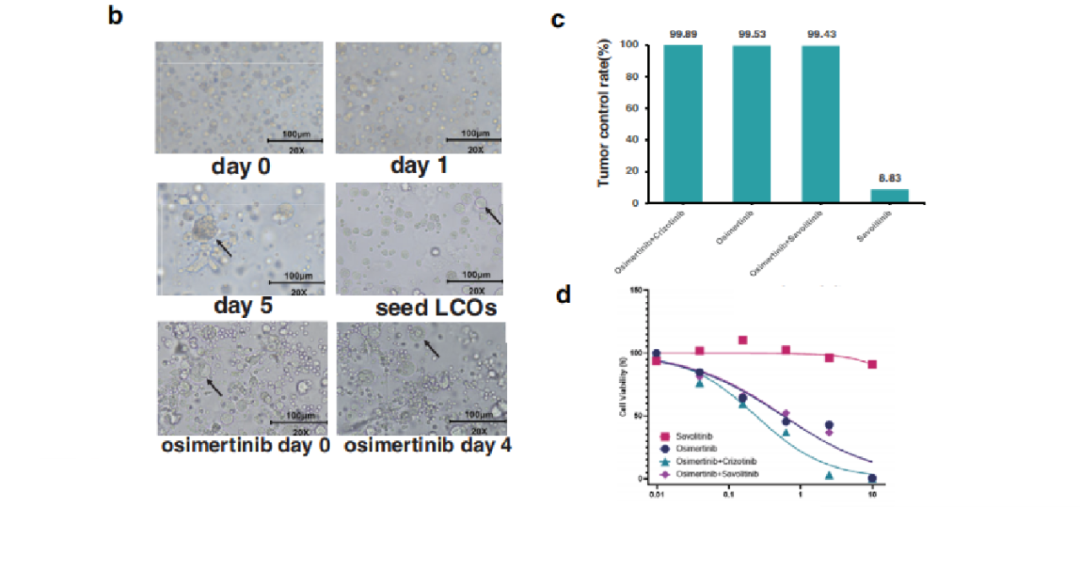
图4. (b)LCOs培养及药敏形态图。(c) 4种不同抗肿瘤药物方案(奥希替尼+克唑替尼/奥希替尼+赛沃替尼/奥希替尼单药/赛沃替尼单药)对LCOs的抑制率。(d) LCOs对4种不同抗肿瘤药物方案处理的剂量-反应曲线。
结论
越来越多的研究提示,患者在对EGFR-TKI治疗产生耐药性后可能发生MET扩增,而本次研究结果进一步表明,与EGFR+/METamp-患者相比,EGFR+/METamp+患者对一线 EGFR-TKI 单药治疗的反应更差,生存率更低(中位PFS:1.9个月 vs. 12.1个月,p<0.001;中位 pOS :11.6个月vs. 25.6个月,p=0.023;中位OS:12.7个月 vs. 33.2个月,p =0.013)。
同时,对恶性胸腔积液来源LCOs 进行的药物敏感性试验能够模拟EGFR+/METamp+和EGFRm肺腺癌患者对 EGFR/MET 双靶向治疗或EGFR单靶向治疗的客观肿瘤反应,为晚期NSCLC患者提供更有前景的一线精准治疗方案。
在本次研究中,不同患者来源LCO模型的药敏结果在临床上与相应患者的肿瘤药物疗效相匹配。EGFR+/METamp+腺癌患者来源LCOs对联合靶向治疗更为敏感,而EGFR+单靶点腺癌患者来源LCOs对奥希替尼和奥希替尼/赛沃替尼或克唑替尼表现出相似的敏感性。这些结果提示,一线EGFR/MET双靶向治疗或许可为EGFR+/METamp+患者提供更有效的精准治疗方案。目前,杨衿记教授团队在LCO模型体外药敏检测体系的辅助下,正在开展一项前瞻性、随机对照临床研究。研究将通过患者临床数据、肺癌类器官模型等分别评估奥希替尼和赛沃替尼联合治疗与奥希替尼单药治疗作为EGFRm合并原发MET扩增的晚期NSCLCs患者的一线治疗的疗效和安全性(FLOWERS研究,NCT05163249),期待该研究结果能够为合并原发MET扩增的EGFRm晚期NSCLC患者带来更好的生存获益。
作者简历
